这吸附理论 死的都能说活了
文献出自Colloids and Surfaces A 应该还算是比较好的杂志了
作者利用干酵母作为生物吸附剂来吸附Cu2+
然后发现pH=4的情况下比pH=5情况下吸附效果还要好
按照一般的思路来说
在不产生Cu沉淀情况下 pH越高吸附效果应该是越好的
越低的话 就存在H+的竞争电位吸附
而作者是这样解释这种现象的:
Increasing pH from 4 to 5 lead to a decrease of adsorption capacity.
This could be attributed to the strong effect of initial concentra-tion of solute which is very high comparing with the relatively low
sorption capacity of biosorbent. Also, parallel precipitation of Cu(II)
hydroxide is possible which means that the initial concentration of
Cu(II) ion is lower than it should be. Besides, increase in density
of the negative charge on the cell surface, causing proton removal
from the solution, thereby decreasing biosorption capacity of Cu(II)
because of competitively adsorption of protons.
第一:我十分不理解作者的第一句话 说初始Cu溶液浓度与吸附剂之比相对而言要大很多 这句话跟主题产生的现象有什么关系?
第二:作者说可能产生水解沉淀 而我通过另外一篇论文看到 Cu的水解电离常数pkb根本在pH=5不存在其他形式的Cu水解产物 具体见如下图形
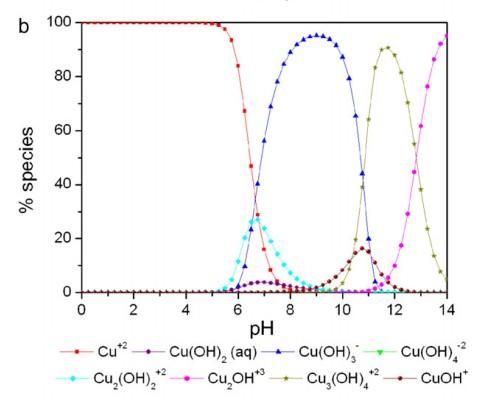
第三:也是最玄乎的一句话 本身你的pH就增大了 照作者这个解释的话 反而吸附剂去质子化了 从而导致还有H+竞争吸附 照这么说 pH低也是竞争吸附 pH高也有竞争吸附
oh 我都
急求高手帮帮我
[ 来自科研家族 木虫环保 ]
[ Last edited by TonyGeN on 2013-4-12 at 21:44 ]![]() 返回小木虫查看更多
返回小木虫查看更多



 京公网安备 11010802022153号
京公网安备 11010802022153号
没怎么看懂,但是楼主精神非常可嘉,支持一下
上面的图真漂亮,不知道是怎么做的
origin就能实现的呀,前提是你要有数据
Cu2+浓度多少?
呵呵,楼主对期刊的文章有点太过认真啦。。。
我的理解是这样的:
第一句话:为后面说明Cu2+产生水解沉淀做铺垫
第二:铜离子形态与pH关系图适合于所有浓度吗?如果不适合,该关系图所采用的Cu2+浓度和本文中Cu2+浓度有何差别?我认为应该是此处c(Cu2+)很高,因而沉淀平衡会在较低的pH(=5)条件下向右移动
第三:文献普遍做出的情况是pH升高可提高Cu2+吸附量,但是本文使用的浓度可能与他们有所差别,我认为作者用pH升高导致氢离子的竞争吸附来解释是不妥的,因为pH升高溶液中的c(H+)理应下降
总之,作者利用pH变化讨论了Cu2+吸附量变化反常理的现象,第二点我可以理解,第三点我和楼主一样,也不能接受,
copper aqueous solutions of initial concen-tration varying from 25 to 200 mg/L
也不是很高呀 很普通的浓度范围