关于西他列汀中间体的合成问题
本人在做西他列汀中间体的时候,一锅法用2,4,5-三氟苯乙酸跟米氏酸形成米氏酸中间体,然后再加入侧链(3-三氟甲基-5,6,7,8-四氢-[1,2,4]三唑[4,3-a]并吡嗪 盐酸盐),加入三氟乙酸维持体系酸性,加热,发现并没有发生反应,米氏酸中间体一直未发生变化。
如果将米氏酸中间体提纯后,再与侧链反应,仍然未检测出反应产物。
请问虫友们做过这个反应吗?问题出在哪?希望虫友们给我答疑解惑。
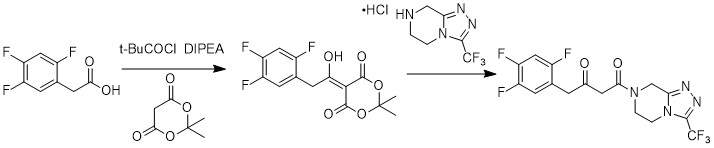
路线.jpg![]() 返回小木虫查看更多
返回小木虫查看更多
今日热帖



 京公网安备 11010802022153号
京公网安备 11010802022153号
这个反应文献上要加酸吗?理论上应该加碱啊
米氏酸中间体跟侧链反应是要酸性的吧,有个加热脱羧的过程
JACS的文献还是很靠谱的,没有发生反应,你走液质了吗?
目前只是通过TLC监测的
应该是侧链先亲核取代,然后开环,加热酸中脱羧。先不要加酸,加入一点水试一下,另外侧链盐酸要中和掉。
首先要确保第一步反应及其彻底性
这是个释放出水的反应,可以参阅类似反应:活泼甲基(图片亚甲基)与醛(羰基)的成烯反应
如上所说,既然有水产生,是就要有去向,图片是用酰氯吸收,释放出的氯化氢由有机胺吸收,如此,反应向生成物方向进行不可逆反应
确保酰氯的质量是关键,体系要干燥无水同样关键,有机碱可以随着反应的进行逐次(少量多次)的加入,因为你一锅煮,碱不要过量太多,否则影响下一步反应,
大胆往下走,没问题的,TLC没分开