【求助】为什么70%乙醇在液相中会有这么多峰?
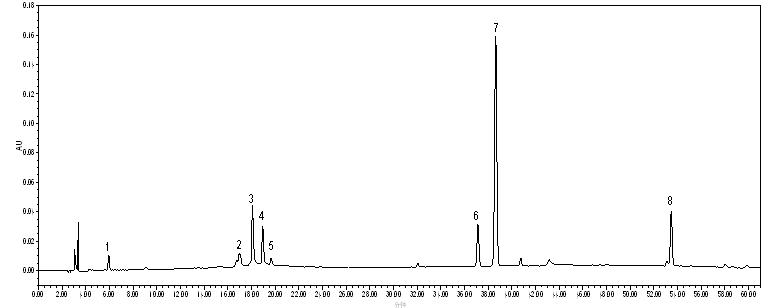
各位虫友麻烦帮我解答一下,我做的是液相指纹图谱,流动相为乙腈-0.2%磷酸,梯度洗脱,乙腈比例从10%变化到100%,采集时间60min。检测波长为215nm。提取药材的溶剂为70%乙醇回流提取。今天进了一针70%乙醇,出现了这么多峰,请有经验的虫友解答一下,谢谢!现附上色谱图一张,其中2、3、4、5为流动相出的峰,在此也想问一下,怎么流动相也会出峰呀(之前有进过空针)?其余为70%乙醇出的峰。本人现在是极度郁闷了
![]() 返回小木虫查看更多
返回小木虫查看更多
今日热帖



 京公网安备 11010802022153号
京公网安备 11010802022153号
图在哪啊?都没看到图
你的乙腈,磷酸,乙醇,以及水(你提到70%乙醇,我假定你用的是乙醇水溶液,含30%的水)都是HPLC级或者色谱级的吗?如果不是,里面带些杂质就很正常了,尤其是磷酸(一般分析纯为85%水溶液)。看你的色谱图里面,很多杂质峰都在0.02AU以上,峰7竟然达到0.16AU,足以造成误分析,说明其中一个或几个溶剂完全不合格,不能用作HPLC。
弄到一些HPLC级的溶剂,你可以依次将上述四种溶剂依次进样,然后一一确定杂质峰的来源。
提取溶剂好像一般都用的是分析纯的吧,如果用色谱基的乙醇太奢侈了吧,乙腈是HPLC级的,水是哇哈哈纯净水,磷酸是分析纯的,都用0.45μ的滤膜过滤过。那这样说起来,我根本就没提出多少峰嘛,sweat:
,
娃哈哈纯净水
去生物系实验室搞一些双蒸水,不会很难吧?肯定比娃哈哈强!那玩意就是过滤后的自来水。还有分析纯磷酸里面杂质太多了。一定要色谱纯的。
用不起色谱纯的乙醇提取,有其他办法。比如在同样的条件下,用色谱纯的乙醇-水作微量提取,专门为HPLC制样,容剂量几毫升就够了。
先确保你的溶剂的纯度吧,拿些进口的试剂看看吧,比如说merck的