| 查看: 8430 | 回复: 27 | |||
| 本帖产生 1 个 QC强帖 ,点击这里进行查看 | |||
| 当前只显示满足指定条件的回帖,点击这里查看本话题的所有回帖 | |||
yjcmwgk禁虫 (文坛精英)
密度泛函·小卒
|
[交流]
【小卒个人文集】写给初学者:小议形式电荷对量化初学者的误导 已有27人参与
|
||
|
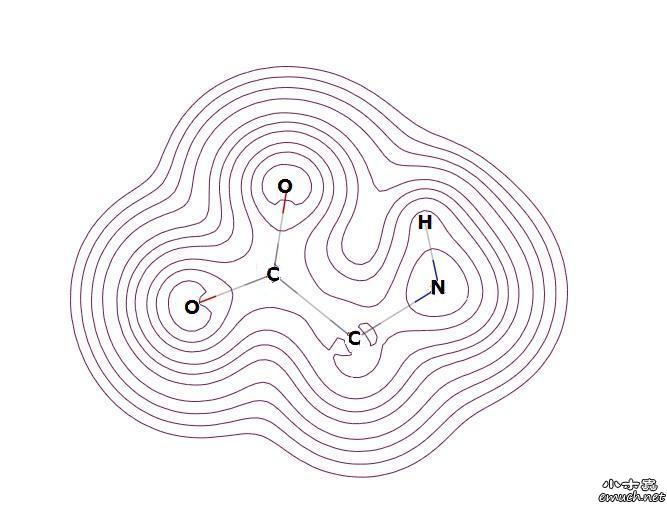
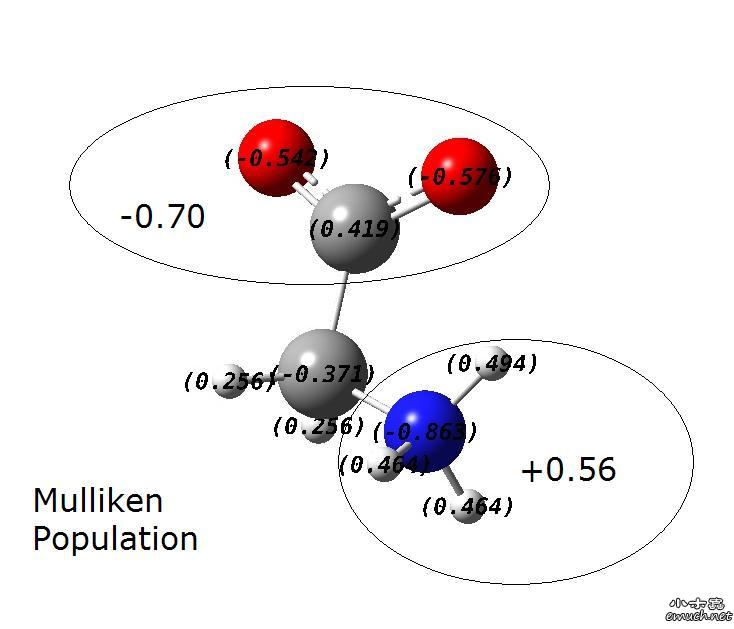
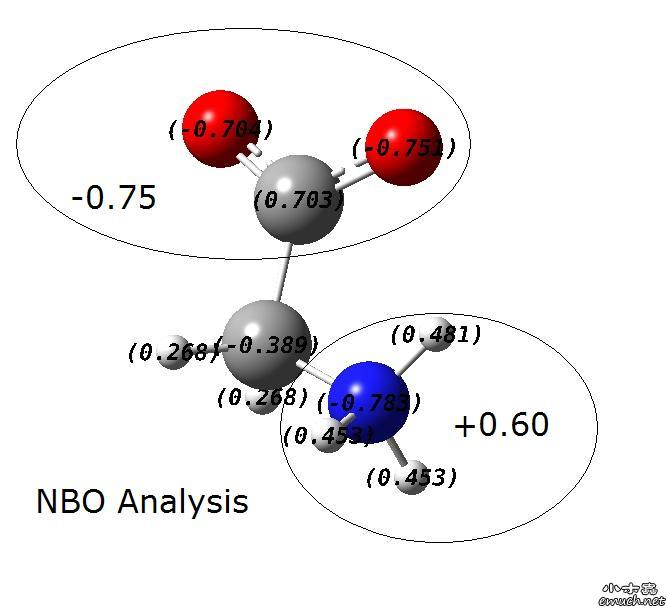
小议形式电荷对量化初学者的误导 经常看到初学量子化学的人,抱着传统化学的形式电荷质疑自己的计算结果。今天又看到新朋友发帖如下: 输入氨基酸的两性离子状态,用BLYP/6-31G和B3LYP/6-31G优化出来的结构都是中性,这是怎么回事?如果我要维持输出为两性离子状态,该如何做呢? 让我回答的话,我会说:你的计算没错儿。氨基酸,整体中型、片段两性。 形式电荷在历史上的巨大贡献我就不多说了。但是,形式电荷就是各组成微粒所带电荷的代数和,由于原子结构中电子排部存在着屏蔽效应和钻穿效应,导致电荷的代数和高低并不能衡量其实质,所以只能称为表观上的电荷分布。在研究化学问题本质的量子化学眼中,形式电荷弊大于利。 十一正好放假,决定助人为乐攒人品。于是我随手计算了一个两性甘氨酸分子。计算水平B3LYP/6-31+G*(因为羧基是强烈的负电中心,所以加弥散函数)。我们就用这个分子为例,来看一下,正统的量子化学是如何理解这种所谓的“两性分子”的。 构型的搭建,严格按照实验生物化学家提出的两性分子的结构式,搭建为(+)NH3CH2COO(-)。计算输入文件如下: 计算之后我们首先看图1。这是整个分子的电子密度图,一般被我们称为electronic density图。在这个图里,明显羧基周围的电子密度高于氨基周围的电子密度。这一点很容易看出:氧周围套的“圈圈”比氮周围多嘛。这种图形,咱们版的zhou2009专家特别擅长。 可是这个图像还不是太直观。为了更直观的理解分子内电荷分布,量子化学家们做了许多种电荷分布的分割方案(这个有个专门的名字,叫做电子布居分析,英文是population analysis。很多人错误的写成了“电子布局分析”,这是不对的)。mulliken、aim、nbo是常用的三种电子布居方式。其中,mulliken最简单;nbo最常用;aim既不是最简单的,也不是最常用的,aim比较尴尬…… 这里面就涉及到了一个量子化学中的电子布居概念与实验化学中的形式电荷概念的冲突了。量子化学从来都认为,电子是不可能完全失去或者完全得到的,量子化学关心的是在空间中的电子云,其电子密度的疏密分布。即使是离子化学物,阳离子也绝对不会将电荷完全给予阴离子。其实说白了,布居分析就是把电子云划分给原子,就说哪个原子“拥有”多少电子而已。比如说经过mulliken布居分析,说某个C原子“拥有”6.23个电子,那么我们就说这个原子的mulliken电荷为(-6.23)-(-6.00)=-0.23。不同的布居分析,就是划分标准的不同而已。 言归正传,我们将图1中所显示的电子密度图用mulliken和nbo两种方式进行布居分析。得到图2和图3。 从图中可以看到,虽然具体数值不同(前文说了,这是不同的布居分析采用不同的划分标准所致),但是羧基明显是吸电子基,是分子内的负电中心,氨基明显是供电子基,是分子内的正电中心。这就够了。量子化学从来不认为电子能够完全得到或者完全失去。能达到±0.4以上,量子化学就认为这已经是非常强的吸电子基团/供电子基团了。 如果我们做出静电势图,我们将会得到更清晰的概念。静电势就是将正电荷从无限远处移到分子周围空间某点所做的功,或者将负电荷从无限远处移到分子周围空间某点所做的功的负值。静电势为正值,则代表该区域更容易吸引负离子,反之则更容易吸引正离子。 图4就是甘氨酸分子的静电势图。可以看出,在一个较大的空间范围内,羧基的一侧明显更容易吸引正离,而氨基的一侧明显更容易吸引负离子。这就是我们量子化学所认为的两性分子。 其实量子化学的布居分析与传统化学的形式电荷并无本质区别。两性分子的概念的本质也就是分子的两个区域更容易与正电荷中心或负电荷中心相结合而已。然而,必须承认的是,量子化学的布居分析比传统化学的形式电荷更容易深入本质。 我只是给刚刚从实验化学那边过来的同仁们开个头罢了。我的讲解太过于简单了,流于表面而已。如果大家想深入了解量子化学对电子结构的理解方式,可以看zhou2009版主的一系列深入浅出的帖子。这些帖子已经被整理为七篇中文论文,发表于《Research of Calculation and Simulation》(中文名《计算与模拟研究》)这个杂志上。 Research of Calculation and Simulation, 2010, Vol. 1, No. 1, Page 34-42. Research of Calculation and Simulation, 2010, Vol. 1, No. 1, Page 43-44. Research of Calculation and Simulation, 2010, Vol. 1, No. 1, Page 80-81. Research of Calculation and Simulation, 2010, Vol. 1, No. 2, Page 122-123. Research of Calculation and Simulation, 2010, Vol. 1, No. 2, Page 132-134. Research of Calculation and Simulation, 2010, Vol. 1, No. 3, Page 192-197. Research of Calculation and Simulation, 2010, Vol. 1, No. 3, Page 198-200. 注释:所有的计算全部使用Gaussian03B01,所有的图形显示全部使用GaussView5.08 [ Last edited by yjcmwgk on 2010-10-5 at 00:56 ] 从sobereva姐那里转引一些内容,以此表达对sobereva姐的崇敬: [ Last edited by yjcmwgk on 2011-5-26 at 11:11 ] |
» 本帖已获得的红花(最新10朵)
» 本帖@通知
» 猜你喜欢
 能源环境新材料研究团队 导师介绍 研究生招生
已经有0人回复
能源环境新材料研究团队 导师介绍 研究生招生
已经有0人回复
 能源环境新材料研究团队 导师介绍 研究生招生
已经有0人回复
能源环境新材料研究团队 导师介绍 研究生招生
已经有0人回复
 物理化学论文润色/翻译怎么收费?
已经有296人回复
物理化学论文润色/翻译怎么收费?
已经有296人回复
 能源环境新材料研究团队 导师介绍 研究生招生
已经有0人回复
能源环境新材料研究团队 导师介绍 研究生招生
已经有0人回复
 348 求调剂
已经有4人回复
348 求调剂
已经有4人回复
 招收 材料、新能源、冶金、化工、环境 等工科类考生
已经有2人回复
招收 材料、新能源、冶金、化工、环境 等工科类考生
已经有2人回复
 招收 新能源、冶金、材料、化工、环境 等工科类考生
已经有0人回复
招收 新能源、冶金、材料、化工、环境 等工科类考生
已经有0人回复
 393求调剂推荐
已经有1人回复
393求调剂推荐
已经有1人回复
 能源环境新材料研究团队 招收 新能源、冶金、材料、化工、环境 等工科类考生
已经有0人回复
能源环境新材料研究团队 招收 新能源、冶金、材料、化工、环境 等工科类考生
已经有0人回复
 能源环境新材料研究团队 招收 新能源、冶金、材料、化工、环境 等工科类研究生
已经有0人回复
能源环境新材料研究团队 招收 新能源、冶金、材料、化工、环境 等工科类研究生
已经有0人回复
 武汉纺织大学教育部重点实验室调剂
已经有0人回复
武汉纺织大学教育部重点实验室调剂
已经有0人回复
» 本主题相关商家推荐: (我也要在这里推广)
jiangbin_ouc
木虫 (正式写手)
- 应助: 1 (幼儿园)
- 金币: 2328.5
- 散金: 110
- 红花: 6
- 帖子: 316
- 在线: 222.8小时
- 虫号: 424835
- 注册: 2007-07-22
- 性别: GG
- 专业: 金属材料的磨损与磨蚀
27楼2013-11-27 19:40:28
mengfc
金虫 (正式写手)
- 应助: 20 (小学生)
- 金币: 1301.2
- 散金: 1807
- 红花: 5
- 帖子: 927
- 在线: 524.4小时
- 虫号: 818484
- 注册: 2009-07-30
- 性别: GG
- 专业: 凝聚态物性 II :电子结构
2楼2010-10-04 21:51:52
★
小木虫(金币+0.5):给个红包,谢谢回帖交流
小木虫(金币+0.5):给个红包,谢谢回帖交流
  |
3楼2010-10-04 22:39:08
4楼2010-10-04 23:40:25
















 回复此楼
回复此楼 涂易
涂易



