求助:金属团簇Fe-NU-1000所带电荷及自旋多重度的判断
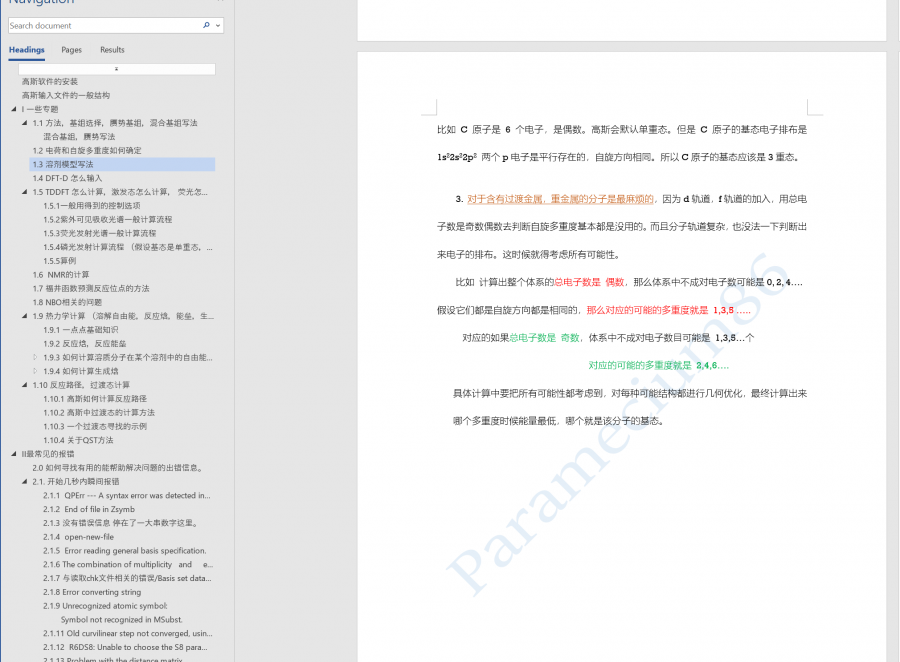
一种负载过渡金属Fe的MOF材料:Fe-NU-1000(见下图),现想对这个团簇进行结构优化,所带电荷和自旋多重度不会判断,想请教各位老师。分子式是C56H54O32FeZr6, 用这种材料催化环己烷脱氢。按照文献给出的计算方法和基组分别为:M06-L泛函;C H O:6-31G(d); Fe Zr:SDD![]() 返回小木虫查看更多
返回小木虫查看更多
今日热帖
一种负载过渡金属Fe的MOF材料:Fe-NU-1000(见下图),现想对这个团簇进行结构优化,所带电荷和自旋多重度不会判断,想请教各位老师。分子式是C56H54O32FeZr6, 用这种材料催化环己烷脱氢。按照文献给出的计算方法和基组分别为:M06-L泛函;C H O:6-31G(d); Fe Zr:SDD![]() 返回小木虫查看更多
返回小木虫查看更多



图贴不上了
首先判断体系的电荷,不要考虑什么金属原子 化合价这种东西。这个跟分子的电荷没有关系。原则上电荷是你自己来规定的。比如你要算Na 你可以设定电荷是0 那么就是告诉高斯你要计算的是 钠原子 ; 你也可以设定+1, 那你要算的就是 钠离子 。你甚至可以设置-1 那你就是告诉高斯去算 Na- 阴离子。 你必须先确定自己要算的是什么,才能确定体系的电荷。比如你这个玩意是个分子。孤立存在的 也没有其他离子跟它在体系里对应。那这就是一个中性的分子。这个体系的电荷就是0 。 这时候不要去看中间有什么金属原子,金属原子什么化合价,这时候把化合价考虑进来就是把自己绕晕了。(也不要把背景电荷和体系的电荷混淆。背景电荷是在分子周围外加一些电荷,不算是分子本身的电荷)

等你确定了电荷你才能去设定自旋多重度。因为自旋多重度完全是根据体系的电子数目来确定的。
体系的电子数目=所有原子本身包含的所有电子-正电荷数目+负电荷数目 所以比如你的体系电荷量是0 那么这个体系的电子数目就等于体系内所有原子所包含电子的总和。
然后根据电子数目去猜测可能的自旋多重度。因为有过渡金属原子一般都要尝试几个不同的多重度 找出能量最低的基态 (总电子数目是偶数可能的多重度就是 1 3 5 7 9。。。; 奇数对应的多重度就是 2 4 6 8.。。等等)
具体可以看我这个教程http://muchong.com/t-14242735-1 第1.2节。截图如下
电荷多重度1.png
电荷多重度2.png
,
最简单的就是数电子数目,总电子数是偶数的,自旋多重度就是1,3,5。。。。。,奇数的就是2,4,6。。。