原核表达蛋白表达量很低,求大神指点!
最近在表达一个蛋白,质粒是直接购买文献中构建好的,如下图所示。

感受态也是用的文献中的Rosetta™ 2(DE3)pLysS,所用的诱导条件也是跟文献保持一致,18℃下IPTG终浓度为0.5mM,诱导16小时,可溶性表达。
然后8000g 4℃离心5 min,弃上清,以20mM Tris-HCl(pH=8.0)重悬沉淀,加入PMSF终浓度为100μg/ml,200W超声1s,停2s,共15 min,然后SDS-PAGE电泳。
但是经过SDS-PAGE电泳检测,蛋白表达量很低,重复好多次了,一直也没办法调整过来,以前做流调出身的新手,现在转行做蛋白,一直做不出来,老板和我都很着急,求大神支招。
其实,我也知道肯定有某些方面我做的跟文献里面不一致,但是我又不知道具体问题出在哪里,很是惆怅啊……
我也怀疑是不是超声破碎的时候蛋白裂解了,但是也不知道如何证实,也不知道如何解决……
就这么多金币,帮我解决了这个问题都送出去算了……
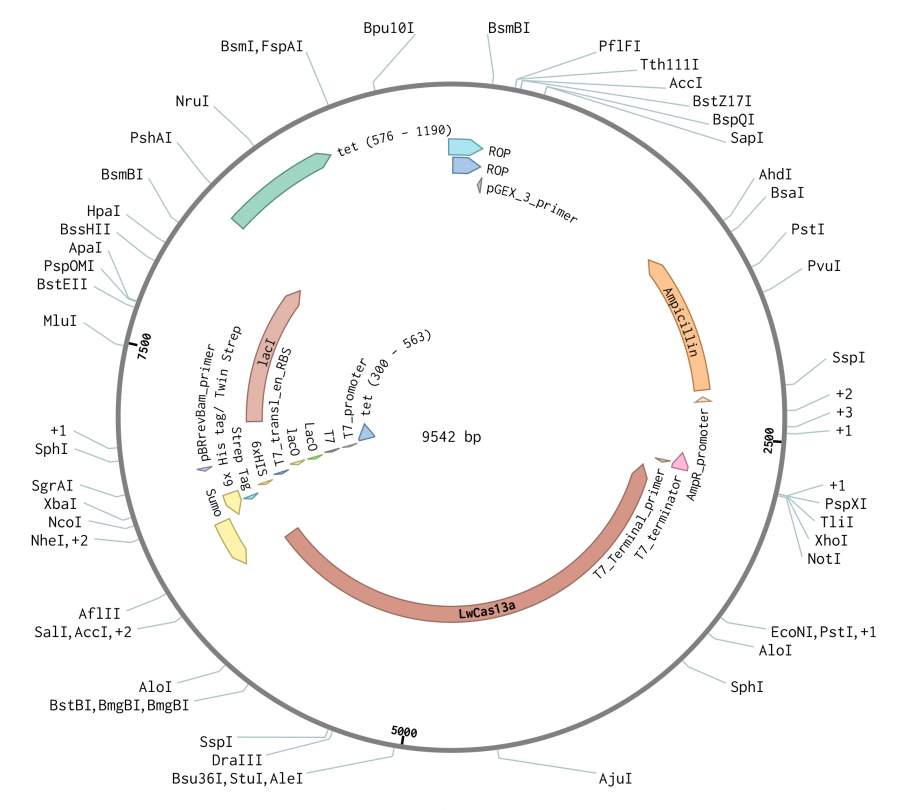
pC013-pET-His6-TwinStrep-SUMO-LwCas13a-sequence.jpg![]() 返回小木虫查看更多
返回小木虫查看更多
今日热帖



 京公网安备 11010802022153号
京公网安备 11010802022153号
楼主,表达分子量大于100kda的重组蛋白,经常会遇到表达量不高的问题。我想这个应该没有更好的解决办法,楼主不如加大发酵规模,然后采用亲和层析加分子筛或离子交换色谱来提纯,后两者我也没有做过哈。
,
Rosetta™ 2(DE3)pLysS的生长温度略低于DE3,33℃左右,用乳糖诱导的效果比IPTG好多了,很多DE3表达很多的酶,plysS几乎没表达的几率还是蛮大的。重点:乳糖诱导
诱导的od是多少
楼主,我是做细菌的,最近也要纯化这个蛋白,楼主可否可以借点这个质粒给我?万分感谢